SEGURA
Vacina de Oxford recebe registro definitivo da Anvisa
O imunizante é produzido e distribuído no Brasil pela Fundação Oswaldo Cruz (Fiocruz)
12/03/2021 às 11:32
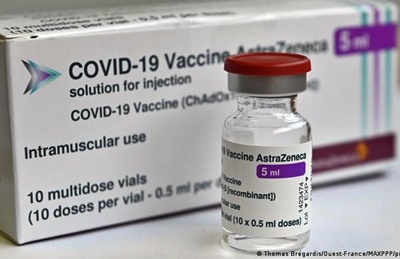 A Agência Nacional de Vigilância Sanitária (Anvisa) concedeu o registro definitivo para a vacina da Universidade de Oxford/AstraZeneca contra o coronavírus. O imunizante é produzido e distribuído no Brasil pela Fundação Oswaldo Cruz (Fiocruz).
A Agência Nacional de Vigilância Sanitária (Anvisa) concedeu o registro definitivo para a vacina da Universidade de Oxford/AstraZeneca contra o coronavírus. O imunizante é produzido e distribuído no Brasil pela Fundação Oswaldo Cruz (Fiocruz).
O gerente-geral de medicamentos da Anvisa, Gustavo Mendes, confirmou que o Brasil será responsável por uma das etapas de desenvolvimento da vacina. Segundo ele, a confecção de parte do imunizante no país representa "maior autonomia e maior acesso à vacina".
No entanto, a vacina autorizada pela agência reguladora brasileira sofre reveses internacionais. Países da Europa -- como a Dinamarca, Islândia e Noruega -- suspenderam o uso da vacina Covid-19 recombinante, desenvolvida pela Oxford/Astrazeneca, depois de pacientes relatarem o surgimento de coágulos após receberem doses do imunizante.
Gustavo Mendes detalhou as etapas em que se encontram as demais vacinas em análise para aplicação na população brasileira. De acordo com a Anvisa, a vacina da farmacêutica Jansen, que teve os estudos da fase clínica e a certificação de boas práticas aprovados, deve encaminhar à agência o pedido de registro ou de autorização de uso emergencial para que seja disponibilizada ao público.
Na avaliação do gerente-geral de medicamentos da Anvisa a vacina da Moderna deverá ser aceita pela agência, apesar do laboratório não ter encaminhado nenhum pedido de autorização de importação, uso emergencial ou registro do imunizante.
Gustavo Mendes disse que as aprovações obtidas pela vacina em agências sanitárias de outros países, como Estados Unidos e Canadá, indicam que ela deve ser aceita no Brasil caso entre com pedidos na Anvisa. Segundo o gerente-geral, os órgãos internacionais compartilham dos mesmos procedimentos adotados nacionalmente.
A Anvisa disse ainda que o laboratório responsável pela Sputnik-V entrou com um pedido de anuência para a realização de estudos clínicos no Brasil, mas a fabricante não respondeu às exigências feitas pelo órgão regulador brasileiro.
Gustavo Mendes afirmou que a agência aguarda o contato da União Química, a representante legal do desenvolvimento do imunizante no Brasil, para que a aprovação seja feita depois da validação dos requisitos. Segundo Medes, o laboratório responsável pela vacina Covaxin também não entrou com um pedido de uso emergencial e estudo clínico no país.
A Anvisa também aprovou nesta sexta-feira (12) o uso do medicamento Rendesivir para pacientes com coronavírus.
Fonte: CNN

Comentários



 A Agência Nacional de Vigilância Sanitária (Anvisa) concedeu o registro definitivo para a vacina da Universidade de Oxford/AstraZeneca contra o coronavírus. O imunizante é produzido e distribuído no Brasil pela Fundação Oswaldo Cruz (Fiocruz).
A Agência Nacional de Vigilância Sanitária (Anvisa) concedeu o registro definitivo para a vacina da Universidade de Oxford/AstraZeneca contra o coronavírus. O imunizante é produzido e distribuído no Brasil pela Fundação Oswaldo Cruz (Fiocruz).

























